Разработка безболезненного автоматизированного пластыря с микроиглами открывает новые перспективы в доставке лекарственных препаратов, в частности, для процедур экстракорпорального оплодотворения (ЭКО). Основная цель инновации заключается в решении проблемы болезненности традиционных инъекций и устранении непоследовательности при самостоятельном введении препаратов, что часто становится главной причиной неудач ЭКО. Устройство запрограммировано на высвобождение гормонов в определенном ритме с использованием технологии световой активации.
Результаты исследования были опубликованы в журнале Small в ноябре 2025 года. Работа объединила открытия двух отдельных лабораторий и проводилась на базе Университета Макгилла в Монреале и Научно-исследовательского центра INRS в Квебеке. Ведущим автором исследования выступила Марта Черрути, химик-материаловед из Университета Макгилла. Идея применения данной технологии именно для ЭКО принадлежала докторанту Вивьен Тэм, хотя изначально команда рассматривала использование разработки для доставки лекарств от рака.
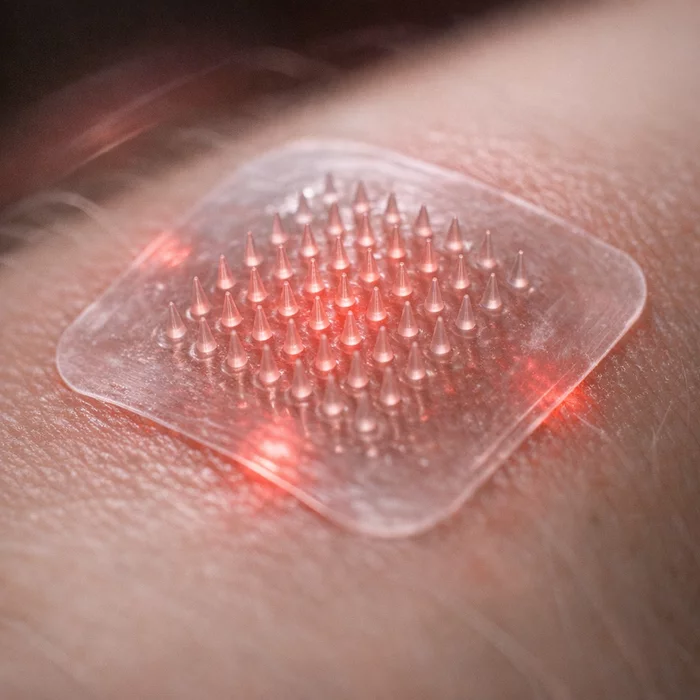
Механизм действия устройства основан на использовании гормона лейпролида. Пластырь состоит из микроигл, изготовленных из нерастворимого синтетического полимера, который не должен разрушаться в организме. Внутри этих игл находятся наночастицы из редкоземельных материалов, наполненные гормоном. Процесс активации запускается низкоэнергетическим светом ближнего инфракрасного диапазона (NIR). Ядро наночастицы преобразует этот свет в более высокоэнергетическое ультрафиолетовое (УФ) излучение, которое разрывает связи в покрытии наночастиц, высвобождая лекарственное средство.
Процедура характеризуется как полностью безболезненная благодаря анатомическим особенностям проникновения микроигл. Иглы прокалывают лишь роговой слой (stratum corneum) — внешний слой мертвых клеток кожи, не проникая достаточно глубоко, чтобы задеть чувствительные нервные окончания. В ходе испытаний на крысах было подтверждено, что гормон успешно попадал в кровеносную систему животных, при этом наночастицы оставались в пластыре и не проникали в организм, что исключило их накопление в печени или других органах. Тесты также подтвердили отсутствие токсичности материалов.
Несмотря на успех первичных испытаний, существуют определенные вызовы и ограничения, отмеченные экспертами, включая Лифэн Кана, доцента Школы фармации Сиднейского университета. Эффективность ближнего инфракрасного света снижается при увеличении объема жировой ткани, что критично, так как традиционные инъекции при ЭКО делаются подкожно. Кроме того, толщина кожи и кровоток варьируются у разных пациентов, что может влиять на физиологическую воспроизводимость результатов.
Существенным барьером для клинического применения остается масштабирование дозировки. В текущих тестах высвобождалась лишь малая доза препарата, недостаточная для терапевтического эффекта у человека. Для решения этой проблемы потребуется увеличение количества пластырей, повышение концентрации наночастиц или создание пластырей большего размера. Также исследователям предстоит сложная задача доказать долговечность полимерных игл и отсутствие их деградации, так как полимеры состоят из водорода, углерода и кислорода — элементов, идентичных составу человеческого тела.
План дальнейших исследований включает проведение дополнительных экспериментов на крысах для проверки эффективности системы в стимулировании созревания яйцеклеток, что еще не было протестировано. В долгосрочной перспективе запланированы испытания на более крупных животных, за которыми последует внедрение в клиническую практику. Это направление развивается на фоне общего тренда на автоматизацию репродуктивных технологий, подтвержденного рождением первого ребенка, зачатого с помощью роботизированного ЭКО, и появлением уникальных видеозаписей имплантации эмбриона человека в реальном времени.

Изображение носит иллюстративный характер
Результаты исследования были опубликованы в журнале Small в ноябре 2025 года. Работа объединила открытия двух отдельных лабораторий и проводилась на базе Университета Макгилла в Монреале и Научно-исследовательского центра INRS в Квебеке. Ведущим автором исследования выступила Марта Черрути, химик-материаловед из Университета Макгилла. Идея применения данной технологии именно для ЭКО принадлежала докторанту Вивьен Тэм, хотя изначально команда рассматривала использование разработки для доставки лекарств от рака.
Механизм действия устройства основан на использовании гормона лейпролида. Пластырь состоит из микроигл, изготовленных из нерастворимого синтетического полимера, который не должен разрушаться в организме. Внутри этих игл находятся наночастицы из редкоземельных материалов, наполненные гормоном. Процесс активации запускается низкоэнергетическим светом ближнего инфракрасного диапазона (NIR). Ядро наночастицы преобразует этот свет в более высокоэнергетическое ультрафиолетовое (УФ) излучение, которое разрывает связи в покрытии наночастиц, высвобождая лекарственное средство.
Процедура характеризуется как полностью безболезненная благодаря анатомическим особенностям проникновения микроигл. Иглы прокалывают лишь роговой слой (stratum corneum) — внешний слой мертвых клеток кожи, не проникая достаточно глубоко, чтобы задеть чувствительные нервные окончания. В ходе испытаний на крысах было подтверждено, что гормон успешно попадал в кровеносную систему животных, при этом наночастицы оставались в пластыре и не проникали в организм, что исключило их накопление в печени или других органах. Тесты также подтвердили отсутствие токсичности материалов.
Несмотря на успех первичных испытаний, существуют определенные вызовы и ограничения, отмеченные экспертами, включая Лифэн Кана, доцента Школы фармации Сиднейского университета. Эффективность ближнего инфракрасного света снижается при увеличении объема жировой ткани, что критично, так как традиционные инъекции при ЭКО делаются подкожно. Кроме того, толщина кожи и кровоток варьируются у разных пациентов, что может влиять на физиологическую воспроизводимость результатов.
Существенным барьером для клинического применения остается масштабирование дозировки. В текущих тестах высвобождалась лишь малая доза препарата, недостаточная для терапевтического эффекта у человека. Для решения этой проблемы потребуется увеличение количества пластырей, повышение концентрации наночастиц или создание пластырей большего размера. Также исследователям предстоит сложная задача доказать долговечность полимерных игл и отсутствие их деградации, так как полимеры состоят из водорода, углерода и кислорода — элементов, идентичных составу человеческого тела.
План дальнейших исследований включает проведение дополнительных экспериментов на крысах для проверки эффективности системы в стимулировании созревания яйцеклеток, что еще не было протестировано. В долгосрочной перспективе запланированы испытания на более крупных животных, за которыми последует внедрение в клиническую практику. Это направление развивается на фоне общего тренда на автоматизацию репродуктивных технологий, подтвержденного рождением первого ребенка, зачатого с помощью роботизированного ЭКО, и появлением уникальных видеозаписей имплантации эмбриона человека в реальном времени.